Le nombre croissant d'infections bactériennes résistantes aux antibiotiques (antibiorésistance), conséquence d'un usage trop large des antibiotiques, a été identifié par l'OMS comme une des principales menaces de santé publique à l'horizon 2050. La phagothérapie, basée sur l'utilisation de virus bactériens (bactériophages), suscite dans ce contexte un vif intérêt. Cependant, pour pouvoir être mise en œuvre, elle requiert d'identifier le phage actif sur une bactérie donnée afin de la détruire. Cette évaluation est aujourd'hui basée sur une détection visuelle des plaques de lyse formées par les bactériophages sur des boîtes de Pétri couvertes de bactéries (
Figure). Cette inspection visuelle, manuelle et excessivement chronophage (12-24h), limite les possibilités d'application de la phagothérapie auprès du patient.
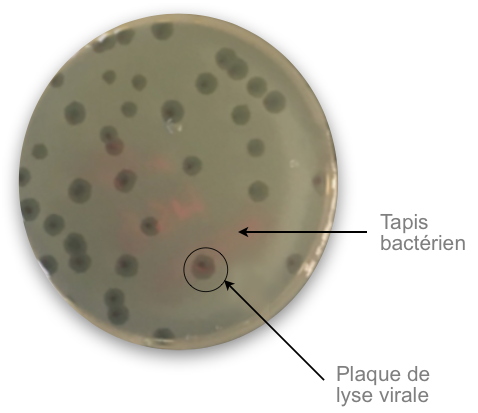 Plaque de lyse.
Plaque de lyse. Pour tester la sensibilité d’une bactérie à un bactériophage, les deux organismes sont co-cultivés à la surface d’une boîte de Pétri recouverte de gélose où un tapis bactérien se forme. Si la bactérie est sensible au bactériophage, celle-ci est détruite (c’est la lyse à proprement parler) et une plage de lyse se forme à la surface de la gélose, au fur et à mesure que la lyse progresse.
© Pheliqs
Une approche originale a été proposée par des chercheurs grenoblois de notre laboratoire, du Département Technologies pour la Biologie et la Santé, du Laboratoire des technologies de la microélectronique, ainsi que des chercheurs suisses [
collaboration réunissant des chercheurs spécialistes de photonique, des biophysiciens et des microbiologistes] pour mettre au point et tester des systèmes optiques afin de vérifier très rapidement l'adéquation phages-bactéries. La stratégie retenue consiste à mettre au point un système d'imagerie sans lentille autour d’un capteur optique de grand format de type CMOS (
Figure). La détection des plaques de lyse est alors basée sur l’utilisation d'un algorithme développé en interne, qui permet de reconstruire les images diffractées par les bactéries afin de remonter en temps réel au nombre et à la cinétique des plaques de lyse. Ces mesures renseignent sur la nature et l'efficacité des phages vis à vis des bactéries et permettent de déterminer leur titre, d'étudier leurs morphologies et leurs cinétiques de croissance. Cette nouvelle approche par imagerie sans lentille présente plusieurs avantages. Tout d'abord, en l'absence de lentilles, la résolution et le champ de vision de l'image sont uniquement limités par le pas des pixels et la taille du capteur. Or, les technologies actuelles tirées par le secteur de l'imagerie numérique permettent la réalisation de très grands capteurs avec de très petits pixels (typiquement plusieurs dizaines de millions de pixels sur un capteur de 24 par 36 mm). Par conséquent, un champ de vision bien plus large que celui de la microscopie optique conventionnelle est accessible pour le suivi de l'interaction phages-bactéries. De plus, comme le pas des pixels des capteurs actuels est de quelques microns seulement, l'imagerie sans lentille permet de résoudre des structures de quelques dizaines de microns, comme des micro-colonies bactériennes naissantes, et donc de gagner du temps dans le processus d'analyse.
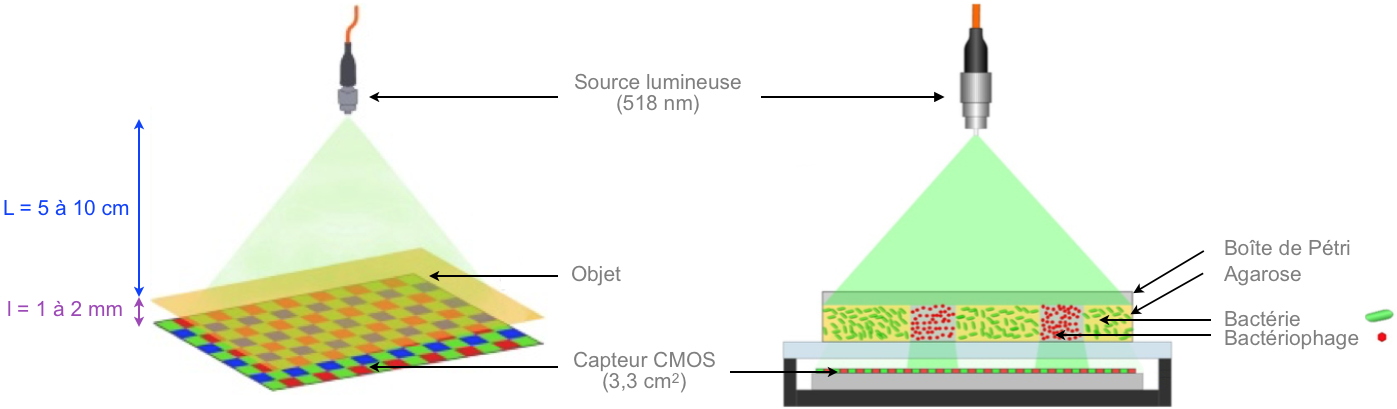 Prototype personnalisé sans lentille.
Prototype personnalisé sans lentille. L'appareil est composé d'un système de détection et d'un module d'illumination. Le système de détection est constitué d'un capteur CMOS (
Complementary Metal Oxide Semiconductor) de 22,3 × 14,9 mm
2 de type APS-C (
Advanced Photo System type-C), issu d'un appareil photo numérique « grand public ». Le capteur est constitué d'une matrice de 5344 × 3516 pixels d'un pas de 4,3 μm. La boîte de Pétri sur laquelle se trouvent les bactériophages est placée directement sur le capteur et éclairée par le haut par une LED verte monochromatique (518 nm) couplée à une fibre optique multimode de 200 μm de diamètre (Thorlabs M72L02). Les images sont acquises directement et converties en fichiers .tiff. Elles sont ensuite traitées à l'aide de deux algorithmes différents ; le premier traite toute la zone de l'image pour détecter les plaques, tandis que le second ne traite qu'une sous-image recadrée de chaque plaque pour calculer le taux de croissance.
© Pheliqs
Grâce à cette technique, les chercheurs rapportent avoir déterminé la sensibilité de
Staphylococcus aureus à différents phage après seulement 3 heures et le titre infectieux après 8 heures et 20 minutes. Ces délais sont bien plus courts que les 12 à 24 heures habituellement nécessaires à l'observation à l'œil nu et au comptage des plaques de lyse. En outre, le suivi continu des échantillons a permis d'étudier la cinétique de croissance des plaques et de confirmer la corrélation entre la densité bactérienne et la diffusion des phages dans la couche de d'agar. Enfin, grâce à la résolution de 4,3 μm (
Figure), les chercheurs ont été en mesure de détecter des micro-colonies bactériennes de
Klebsiella pneumoniae résistantes aux phages à l'intérieur des limites des plaques de lyse, montrant ainsi que leur prototype est également un dispositif approprié pour le suivi de la résistance aux phages.
Cette première preuve de concept d'un système d'imagerie sans lentille, mis en œuvre sous la forme d’un dispositif compact et économique, ouvre une voie prometteuse à la phagothérapie. Plusieurs programmes démarrent au plan national et international pour en valider les applications. Des travaux futurs porteront également sur le développement d'algorithmes plus fins permettant la classification morphologique des plaques (et donc des phages) en fonction de leur taux de croissance mais aussi de leur morphotype.
Collaboration : Laboratoire Photonique Électronique et Ingénierie Quantiques (Irig, CEA-Grenoble, France) ; Laboratoire des Systèmes d'Imagerie pour le Vivant (Leti-DTBS, CEA-Grenoble, France) ; Laboratoire des technologies de la microélectronique (CNRS, France) ; laboratoire de bactériophages et de phagothérapie (Centre hospitalier universitaire vaudois, Suisse).